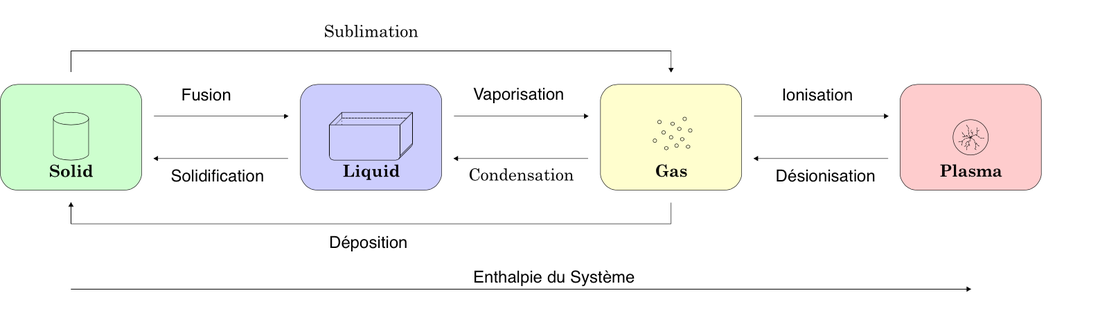
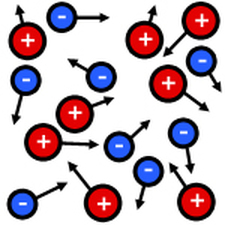
L’effet des variations de température expliqué par la théorie atomique
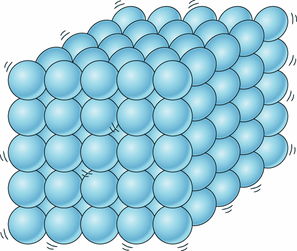
À basse température, les motions des particules diminue et les substances ont moins d’énergie. Les particules sont dans des états de basse énergie et se déplace très peu; les caractéristique de l’état solide.
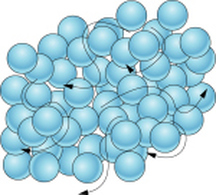
Lorsque la température augmente, l’énergie thermique ajouté est appliquée sur les parties constituantes d’un solide, ce qui provoque le mouvement des particules. Les particules commencent à pousser contre les unes à l’autres et le volume du substance augmente. Le substance est entré dans l’état liquide.
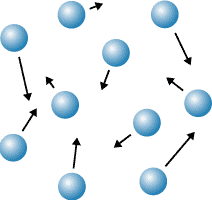
Un état gazeux existe lorsque les molécules ont absorbé tellement d’énergie thermique dû à l’augmentation de la température qu’ils sont libres de se déplacer autour de les unes à l’autres à des vitesses élevées.
Une substance peuvent changer de solide à gaz ou de gaz à solide si la température exposé change très vite. Si la pression est constant, l’état de la substance dépend sur la température qu’elle est exposé à. Comme quand la glace sort d’un congélateur, elle fond, quand l’eau bouille dans un pot, si la température est laissé à un haut température pour trop longtemps.
Une transition de phase est le transformation d’un système thermodynamique d’une phase ou une matière à une autre par la transmission de chaleur. Utilisé pour décrire les transitions entre les solides, liquides et gaz, dans des rares cas, le plasma. Pendant la transition de phase, il y a presque toujours des changements comme la température, la pression et d’autres facteurs. Comme un liquide peuvent devenir gaz, lors du chauffage à la température d’ébullition, ce qui cause un changement du volume. Le point triple d'une substance est la température et la pression à laquelle les trois phases (gaz, liquide et solide) de cette substance coexistent. Par exemple, le point triple de mercure se produit à une température de -38,83440 ° C et une pression de 0,2 MPa.
Lorsque la température augmente, l’énergie thermique ajouté est appliquée sur les parties constituantes d’un solide, ce qui provoque le mouvement des particules. Les particules commencent à pousser contre les unes à l’autres et le volume du substance augmente. Le substance est entré dans l’état liquide.
Un état gazeux existe lorsque les molécules ont absorbé tellement d’énergie thermique dû à l’augmentation de la température qu’ils sont libres de se déplacer autour de les unes à l’autres à des vitesses élevées.
Une substance peuvent changer de solide à gaz ou de gaz à solide si la température exposé change très vite. Si la pression est constant, l’état de la substance dépend sur la température qu’elle est exposé à. Comme quand la glace sort d’un congélateur, elle fond, quand l’eau bouille dans un pot, si la température est laissé à un haut température pour trop longtemps.
Une transition de phase est le transformation d’un système thermodynamique d’une phase ou une matière à une autre par la transmission de chaleur. Utilisé pour décrire les transitions entre les solides, liquides et gaz, dans des rares cas, le plasma. Pendant la transition de phase, il y a presque toujours des changements comme la température, la pression et d’autres facteurs. Comme un liquide peuvent devenir gaz, lors du chauffage à la température d’ébullition, ce qui cause un changement du volume. Le point triple d'une substance est la température et la pression à laquelle les trois phases (gaz, liquide et solide) de cette substance coexistent. Par exemple, le point triple de mercure se produit à une température de -38,83440 ° C et une pression de 0,2 MPa.
Le domaine de la physique qui décrit les caractéristiques et les propriétés des atomes qui composent la matière est formulée par l’anglais John Dalton (1766-1844) au début du 18 siècle.
Le solide:
Un solide ne peuvent pas prendre la forme du récipient dans lequel on la place. Il a une résistance qu’il oppose à une force mécanique ou une force de cisaillement exercée sur sa surface. les particules sont compactées et maintenues dans une structure rigide par la force d’attraction. Elles peuvent bouger, mais seulement par vibration sur place. Le réchauffement d’un solide active les particules, qui vibrent plus rapidement. À température haute, toute matière se présente à l’état fluide parce que la force d’attraction ne peut retenir les particules ensembles et à température baisse, généralement vers l’état solide. À la pression atmosphérique, tous les corps (à l’exception de l’hélium) peuvent se présenter à l’état solide
Un solide ne peuvent pas prendre la forme du récipient dans lequel on la place. Il a une résistance qu’il oppose à une force mécanique ou une force de cisaillement exercée sur sa surface. les particules sont compactées et maintenues dans une structure rigide par la force d’attraction. Elles peuvent bouger, mais seulement par vibration sur place. Le réchauffement d’un solide active les particules, qui vibrent plus rapidement. À température haute, toute matière se présente à l’état fluide parce que la force d’attraction ne peut retenir les particules ensembles et à température baisse, généralement vers l’état solide. À la pression atmosphérique, tous les corps (à l’exception de l’hélium) peuvent se présenter à l’état solide
Liquide:
Un liquide, le liquide le plus cohésif non métallique, prend la forme de la parti du récipient qui le contient et n’est pas fixé dans un position. C’est un fluide incompressible qui se conforme à la forme de son contenant mais conserve une (ou presque) un volume constant et indépendant de la pression. Le volume est certain si la température et la pression son constante. Les particules sont légèrement moins pressées les unes contre les autres que dans un solide. Le liquide est moins dense. Plus un liquide est chauffé, plus rapide est le déplacement de ses particules. Il n’y a plus de force d’attraction. Les particules peuvent donc bouger dans toutes les directions. La masse volumique s’abaisse. À la fin, les particules s’échappent du liquide et forment un gaz.
En plus, ils ont une tension superficielle. Une très fine couche de particules qui sont fortement attirés les unes des autres que a des particules qui les entourent. Si ils ne sont pas dérangé, ils peuvent être très forte. Ils sont assez fort pour supporter la masse d’un insecte comme un araignées d’eau.
Gaz:
Le gaz s’empresse d’envahir tout le volume qu’on lui offre. Il non seulement conforme à la forme de son contenant mais il permettra également a s’agrandir pour remplir le récipient. Le gaz est un fluide compressible et la distance typique entre les particules est plus grande que la taille du particule. Un gaz peut être liquéfié par compression seule, sans refroidissement. Un fluide supercritique (SCF) est un gaz dont la température et la pression sont en haut de la température critique et la pression critique. Dans ce état, la distinction entre le liquide et le gaz disparaît. Par exemple, le dioxyde de carbone supercritique est utilisé pour extraire de la caféine dans la fabrication de café décaféiné.
Le gaz est généralement converti au plasma, soit à partir d’une différence de tension entre deux points énorme, ou en l’exposant à des températures extrêmement élevées. Chauffage des matière à températures très élevées provoque les électrons de quitter les particules, ce qui entraîne la présence des électrons libres.
Plasma:
Le plasma est composé de groupes de particules positivement et négativement chargées. Il n’a pas de forme ou de volume précis et ils sont électriquement conductrice, produit des champs magnétiques et des courants électriques et répond fortement aux forces électromagnétiques. Ls électrons sont arrachés de leurs noyaux, formant un «mer» d’électron. Cela lui donne la capacité à conduire l’électricité. Par exemple, les étoiles, le soleil, l’éclair, gaz à basse pression à l’intérieur des lumière fluorescente et les enseigne au néon, l’ionosphère de la terre, vent solaire etc.

Qui est John Dalton?
John Dalton est né en 1766 et il est mort le 26 juillet 1844. Il était né dans une famille modeste Quaker à Eaglesfield, Angleterre. Pour la plupart de sa vie son travaille était un professeur et conférencier publique, commencé dans son école de village à l’âge de 12 ans. Il faisait parti du société Manchester littéraire et philosophique. Il a fourni un environnement intellectuel stimulant et des installations de laboratoire. Pendant les années 1800, il était la première scientiste a expliqué le comportement des atomes en termes de la mesure de poids. La fascination de Dalton, avec du gaz, lui a conduit à affirmer que toute forme de matière (solide, liquide ou gaz) constitue de petites particules individuelles. Il a créé la première tableau des poids atomiques et il est devenu le premier scientifique à expliquer le comportement des atomes en termes de mesure du poids.
John Dalton est né en 1766 et il est mort le 26 juillet 1844. Il était né dans une famille modeste Quaker à Eaglesfield, Angleterre. Pour la plupart de sa vie son travaille était un professeur et conférencier publique, commencé dans son école de village à l’âge de 12 ans. Il faisait parti du société Manchester littéraire et philosophique. Il a fourni un environnement intellectuel stimulant et des installations de laboratoire. Pendant les années 1800, il était la première scientiste a expliqué le comportement des atomes en termes de la mesure de poids. La fascination de Dalton, avec du gaz, lui a conduit à affirmer que toute forme de matière (solide, liquide ou gaz) constitue de petites particules individuelles. Il a créé la première tableau des poids atomiques et il est devenu le premier scientifique à expliquer le comportement des atomes en termes de mesure du poids.
Référence Bibliographie:
http://fr.wikipedia.org/wiki/Transition_de_phase
http://www.ehow.com/info_8601348_effect-temperature-states-matter.html
http://www.universalis.fr/encyclopedie/matiere-physique-etat-solide/#
http://www.chem4kids.com/files/matter_solid.html
http://www.livescience.com/46972-liquids.html
http://en.wikipedia.org/wiki/State_of_matter
http://www.chem4kids.com/files/matter_plasma.html
http://fr.wikipedia.org/wiki/Transition_de_phase
http://www.ehow.com/info_8601348_effect-temperature-states-matter.html
http://www.universalis.fr/encyclopedie/matiere-physique-etat-solide/#
http://www.chem4kids.com/files/matter_solid.html
http://www.livescience.com/46972-liquids.html
http://en.wikipedia.org/wiki/State_of_matter
http://www.chem4kids.com/files/matter_plasma.html